Электроэпиляция
Содержание:
- Получение марганцовка
- Химические свойства
- Метиленовая синь инструкция по применению
- Обработка марганцовкой клубней и луковиц
- Мифы о лечении содой
- Химические свойства
- Цена Марганцовки. Где взять Перманганат калия?
- Применение марганцовки при размножении растений
- Химические свойства
- Взаимодействие
- Как развести марганцовку для обработки в медицинских целях
Получение марганцовка
Раствор марганцовки
Получение марганцовки в промышленности связано с электролизом концентрированного раствора гидроксида калия с марганцевым анодом. В процессе электролиза материал анода постепенно растворяется с образованием знакомого всем фиолетового раствора, содержащего перманганат-ионы. На катоде происходит выделение водорода. Умеренно растворимый в воде перманганат калия (марганцовка) выделяется в виде осадка.
Было бы заманчиво вместо привычной марганцовки производить перманганат натрия, ведь гидроксид натрия доступнее, чем гидроксид калия. Однако в этих условиях выделить перманганат натрия NaMnO4 невозможно: в отличие от перманганата калия KMnO4, он прекрасно растворим в воде (при 20 °С его растворимость составляет 144 г на 100 г воды).
В нейтральной или слабощелочной среде марганцовка (перманганат) переходит в гидратированный оксид марганца:
2КМnО4+Н2О+3K2SO3→ 2MnO2+3K2SO4+2КОН.
Перманганата калия. Восстановление в щелочной (2), нейтральной (3), кислой (4) среде
В нейтральной или слабощелочной среде перманганат-ион (марганцовка) восстанавливается до оксида марганца (IV):
MnО4+2Н2О+3е → MnО2+4ОН-. Особенно ярко марганцовка проявляет окисляющую способность в кислой среде:
MnО-4+8Н++5е → Mn2++4Н2О.
Подкисленный крепкий раствор перманганата буквально сжигает многие органические соединения, превращая их в углекислый газ и воду. Этим иногда пользуются химики для мытья лабораторной посуды, сильно загрязнённой плохо смываемыми остатками органических веществ.
Твёрдый перманганат калия и его крепкие растворы могут быть опасны. При отравлении концентрированным раствором марганцовки возникает ожог рта, пищевода и желудка. Если вдруг Вы глотнули такой раствор, надо немедленно промыть желудок теплой водой с добавлением активированного угля. Для этого можно также использовать раствор, содержащий в двух литрах воды полстакана слабого раствора (H2O2) и один стакан столового уксуса. В этом случае ионы марганца переходят в менее опасные катионы марганца, а сама химическая реакция протекает следующим образом:
2KMn04+5H2O2+6CH3COOH→ 2Mn(CH3COO)2+5O2+2CH3COOK+8H2O
Химические свойства
| Окисленная форма | Восстановленная форма | Среда | E, В |
|---|---|---|---|
| MnO4− | MnO42− | OH− | +0,56 |
| MnO4− | H2MnO4 | H+ | +1,22 |
| MnO4− | MnO2 | H+ | +1,69 |
| MnO4− | MnO2 | OH− | +0,60 |
| MnO4− | Mn2+ | H+ | +1,51 |

Слева направо (водные растворы): Co(NO3)2 (красный); K2Cr2O7 (оранжевый); K2CrO4 (жёлтый); NiCl2 (бирюзовый); CuSO4 (голубой); KMnO4 (фиолетовый)
Раствор KMnO4 в воде в мерной колбе
Является сильным окислителем. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия):
в кислой среде:
- 2KMnO4+5K2SO3+3H2SO4⟶6K2SO4+2MnSO4+3H2O{\displaystyle {\ce {2KMnO4 + 5K2SO3 + 3H2SO4 -> 6K2SO4 + 2MnSO4 + 3H2O}}};
в нейтральной среде:
- 2KMnO4+3K2SO3+H2O⟶3K2SO4+2MnO2+2KOH{\displaystyle {\ce {2KMnO4 + 3K2SO3 + H2O -> 3K2SO4 + 2MnO2 + 2KOH}}};
в щелочной среде:
- 2KMnO4+K2SO3+2KOH⟶K2SO4+2K2MnO4+H2O{\displaystyle {\ce {2KMnO4 + K2SO3 + 2KOH -> K2SO4 + 2K2MnO4 + H2O}}}.
Однако последняя реакция (в щелочной среде) идёт по указанной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
- 2KMnO4+H2SO4⟶K2SO4+Mn2O7+H2O{\displaystyle {\ce {2KMnO4 + H2SO4 -> K2SO4 + Mn2O7 + H2O}}}.
При этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4{\displaystyle {\ce {MnO3HSO4}}}. По реакции с фторидом иода(V) можно получить аналогичный оксофторид:
- KMnO4+IF5⟶KF+IOF3+MnO3F{\displaystyle {\ce {KMnO4 + IF5 -> KF + IOF3 + MnO3F}}}.
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
- 2KMnO4→∘tK2MnO4 +MnO2 +O2{\displaystyle {\ce {2KMnO4->K2MnO4\ +MnO2\ +O2}}}.
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
- 5KMnO4→∘tK2MnO4 +K3MnO4 +3MnO2 +3O2{\displaystyle {\ce {5KMnO4->K2MnO4\ +K3MnO4\ +3MnO2\ +3O2}}}.
Реагирует с солями двухвалентного марганца, например:
- 2KMnO4+3MnSO4+2H2O⟶5MnO2+K2SO4+2H2SO4{\displaystyle {\ce {2KMnO4 + 3MnSO4 + 2H2O -> 5MnO2 + K2SO4 + 2H2SO4}}}.
Эта реакция в принципе обратна дисмутации (диспропорционирование) K2MnO4{\displaystyle {\ce {K2MnO4}}} на MnO2{\displaystyle {\ce {MnO2}}} и KMnO4{\displaystyle {\ce {KMnO4}}}.
Окисляет органические вещества. В частности, разбавленные растворы перманганата калия в щелочной и нейтральной среде окисляют алкены до диолов (реакция Вагнера):
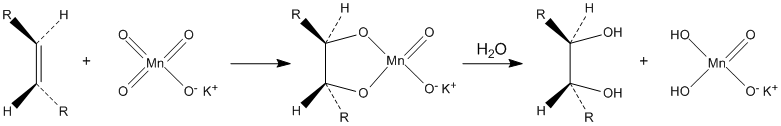
Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
При смеси с пероксидом водорода протекает следующая реакция:
- 2KMnO4+3H2O2⟶2MnO2+3O2↑+2H2O+2KOH{\displaystyle {\ce {2KMnO4 +3H2O2 -> 2MnO2 + 3O2 ^ + 2H2O + 2KOH}}}.
Перманганат калия реагирует с концентрированной соляной, бромоводородной или иодоводородной кислотой. В результате выделяются свободные галогены:
- 2KMnO4+16HCl⟶2KCl+2MnCl2+5Cl2↑+8H2O{\displaystyle {\ce {2KMnO4 + 16HCl -> 2KCl + 2MnCl2 + 5Cl2 ^ + 8H2O}}}
Во время химической реакции хлорид-анион Cl−{\displaystyle {\ce {Cl^{-}}}} окисляется до элементарного хлора, а ион Mn7+{\displaystyle {\ce {Mn^{7+}}}} в перманганат-анионе восстанавливается до катиона Mn2+{\displaystyle {\ce {Mn^{2+}}}}:
- 2Cl−⟶Cl2↑{\displaystyle {\ce {2Cl^{-}-> Cl2 ^}}}
- Mn7+⟶Mn2+{\displaystyle {\ce {Mn^{7+}-> Mn^{2+}}}}
Метиленовая синь инструкция по применению
Метиленовую синь используют для наружного применения. Она очень эффективна при пиодермии, ожогах, фолликулитах и других заболеваниях кожного покрова. А также её водный раствор назначают при лазерном удалении папиллом.
Применение водного раствора распространяется на лечение воспалительных процессов мочевыводящих путей. Обычно это цистит и уретрит. Раствор применяется в качестве средства для промывания. Инструкция также указывает на то, что метиленовая синь помогает при диагностике почек, т. к. после внутреннего применения, моча приобретает синий цвет.
При отравлениях метиловую синь вводят внутривенно. Для лечения разных групп недугов следует делать растворы разной концентрации.
- При наружном применении используется спиртовой раствор 1–3%. Поражённые места обрабатывают ватным тампоном.
- Цистите и уретрите применяют водный раствор 0,002% в соотношении (1:5000). Им следует промывать половые органы.
- Отравлении окисью углерода различными цианидами и сероводородом, делают водный раствор 1% и вводят внутривенно, в количестве 50–100 мл при отравлении метгемоглобинообразующими ядами и анилином, метиленовую синь применяют в более малых дозах, это 0,1– 0,15 мл/кг., раствор также 1%. При отравлении угарным газом используется с активированным углем.
Норма дозировки для взрослого человека, при приёме внутрь, 0,1 гр. 3–4 раза в день, а для детей норма меняется в зависимости от возраста, это от 0,005 до 0.01 гр. 3–4 раза в день.
При современных технологиях по источникам информации, была выявлена эффективность метиленового синего при лечении болезни Альцгеймера. Но изучение этого явления ещё продолжается до полного подтверждения.
Обработка марганцовкой клубней и луковиц
Клубни и луковицы растений уязвимы перед различными заболеваниями, поэтому не лишним будет обработать их раствором марганцовки. Процедура эта достаточно кропотливая, но эффективная. Опытные дачники проводят ее каждую весну.
Особенно хорошо зарекомендовала себя обработка лука перед посадкой марганцовкой. Такая процедура обеззараживает луковицы и одновременно ускоряет развитие корневой системы.
Лук в марганцовке перед посадкой можно замочить, например, таким способом: в 1 л воды растворите 3 г вещества и поместите луковицы в раствор на 1 час. Если на посадочном материале заметны признаки заражения, готовят более мощное средство. В 1 л воды добавляют 20 г вещества и замачивают луковицы на 20 минут.
Картофельные клубни замачивают на 20-30 минут в обеззараживающем растворе. Для его приготовления разведите в 10 л воды 10 г марганцовки. Чтобы усилить защитное действие, добавьте в раствор 2 г медного купороса. Также эффективно проводить опрыскивание препаратом.
Можно замачивать в растворе марганцовки луковицы тюльпанов, нарциссов, гладиолусов, крокусов и других луковичных и клубнелуковичных растений. При этом жидкость должна полностью покрывать луковицы.
Мифы о лечении содой
В интернете пишут, что сода помогает избавиться от алкоголизма, курения, наркомании, лечит болезни почек, печени, женских половых органов, мигрень, улучшает внимательность и успеваемость у детей, выводит шлаки (которых не существует) и даже избавляет от раковых опухолей. При этом она дёшево стоит и продаётся в каждом продуктовом магазине. Было бы прекрасно, если бы у человечества действительно было такое потрясающее лекарство. Но сода не панацея, и принимать внутрь её не нужно: это не только не принесет пользы, но и может навредить. Разберемся, откуда взялись все эти мифы о пользе соды и что с ними не так.
Миф №1. Сода применяется для профилактики и лечения рака
Сода не лечит рак – нет ни одного компетентного, рецензируемого исследования, которое бы это подтвердило. Лечение рака содой особенно опасно: некоторые виды рака хорошо поддаются химиотерапии или операбельны, но люди упускают драгоценное время.
Появился этот лженаучный метод лечения во многом благодаря бывшему врачу-онкологу Туллио Симончини, на которого обычно и ссылаются на сайтах с подобными рекомендациями. Он считал, что рак вызывается грибами рода Candida, что неверно. Симончини прописывал своим онкобольным уколы содового раствора вместо настоящей терапии, за что его лишили права заниматься медицинской деятельностью. Но это его не остановило, и он открыл свое заведение, где продолжил практиковать содолечение. Из-за такого лечения погиб 27-летний юноша Лука Оливотти. В январе 2018 года Туллио Симончини приговорили к 5,5 годам тюрьмы за убийство и ненадлежащую врачебную практику.
Для профилактики рака сода тоже бесполезна: рак вызывается накоплением мутаций в клетках, а не грибами. Поэтому защитить от рака сода не может.
Суть мифа – сода, а также некоторые продукты питания помогают держать в равновесии кислотно-щелочной баланс в организме. Существуют даже целые списки продуктов, которые «ощелачивают» или «закисляют» организм, с рекомендациями сколько их есть и когда. Существует много разных списков «защелачивающих» и «закисляющих» продуктов. Согласно спискам, большинство овощей полезны, потому что ощелачивают.
Кислотно-щелочной баланс (также применяются термины «кислотно-основное» или «кислотно-щелочное равновесие», «равновесие кислот и оснований») – действительно существующее явление. Он отражает постоянство соотношения кислот и оснований во внутренней среде организма, его количественно измеряют знакомым нам водородным показателем – pH. Разные химические реакции в организме происходят при разных уровнях pH, а ткани очень чувствительны к его перепадам, поэтому даже небольшие изменения могут привести к гибели клеток и нарушению работы ферментов.
Из-за таких нарушений возможен летальный исход. Если бы такой важный механизм контролировался извне продуктами, которые ест человек, то вряд ли бы наш вид вообще выжил. К счастью, для контроля уровня pH у нас есть свои механизмы, среди которых буферные системы крови, а также дыхательная и мочевыделительная системы. В комплексе всё это мощная система, которая помогает организму саморегулировать постоянство своей среды. Нарушение в функционировании любого компонента этой системы потребует медицинской помощи.
Сода не просто не поможет регулировать кислотно-щелочной баланс, а наоборот, может его нарушить. За счёт накопления щелочных веществ может увеличиться уровень pH крови – это называется алколозом. Алколоз опасен и требует медицинской помощи, поскольку уменьшается мозговой и коронарный кровоток, снижаются артериальное давление и минутный объём крови, нарастает нервно-мышечная возбудимость, возможны обмороки и судороги, снижение моторики кишечника и активности дыхательного центра.
Миф №3. Сода помогает худеть и чиститься от шлаков
Сода не поможет похудеть без вреда здоровью. После курса приёма соды можно приобрести проблемы с желудочно-кишечным трактом, дисбаланс электролитов, получить кислотный рикошет – и похудеть вследствие этих проблем.
Существование шлаков не доказано вообще никем, это понятие использует только альтернативная медицина (к ней относятся все способы лечения, эффективность и безопасность которых не доказана научным методом). У человека есть почки и печень: их достаточно, чтобы нейтрализовать вредные продукты обмена веществ. Если в организм попадут отравляющие вещества, человеку потребуется медицинская помощь.
Мифы о похудении: что нужно знать, чтобы впустую не тратить деньги
Химические свойства
| Окисленная форма | Восстановленная форма | Среда | E, В |
|---|---|---|---|
| MnO4− | MnO42− | OH− | +0,56 |
| MnO4− | H2MnO4 | H+ | +1,22 |
| MnO4− | MnO2 | H+ | +1,69 |
| MnO4− | MnO2 | OH− | +0,60 |
| MnO4− | Mn2+ | H+ | +1,51 |
Слева направо (водные растворы): Co(NO3)2 (красный); K2Cr2O7 (оранжевый); K2CrO4 (жёлтый); NiCl2 (бирюзовый); CuSO4 (голубой); KMnO4 (фиолетовый)
Раствор KMnO4 в воде в мерной колбе
Является сильным окислителем. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия):
в кислой среде:
- 2KMnO4+5K2SO3+3H2SO4⟶6K2SO4+2MnSO4+3H2O{\displaystyle {\ce {2KMnO4 + 5K2SO3 + 3H2SO4 -> 6K2SO4 + 2MnSO4 + 3H2O}}};
в нейтральной среде:
- 2KMnO4+3K2SO3+H2O⟶3K2SO4+2MnO2+2KOH{\displaystyle {\ce {2KMnO4 + 3K2SO3 + H2O -> 3K2SO4 + 2MnO2 + 2KOH}}};
в щелочной среде:
- 2KMnO4+K2SO3+2KOH⟶K2SO4+2K2MnO4+H2O{\displaystyle {\ce {2KMnO4 + K2SO3 + 2KOH -> K2SO4 + 2K2MnO4 + H2O}}}.
Однако последняя реакция (в щелочной среде) идёт по указанной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
- 2KMnO4+H2SO4⟶K2SO4+Mn2O7+H2O{\displaystyle {\ce {2KMnO4 + H2SO4 -> K2SO4 + Mn2O7 + H2O}}}.
При этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4{\displaystyle {\ce {MnO3HSO4}}}. По реакции с фторидом иода(V) можно получить аналогичный оксофторид:
- KMnO4+IF5⟶KF+IOF3+MnO3F{\displaystyle {\ce {KMnO4 + IF5 -> KF + IOF3 + MnO3F}}}.
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
- 2KMnO4→∘tK2MnO4 +MnO2 +O2{\displaystyle {\ce {2KMnO4->K2MnO4\ +MnO2\ +O2}}}.
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
- 5KMnO4→∘tK2MnO4 +K3MnO4 +3MnO2 +3O2{\displaystyle {\ce {5KMnO4->K2MnO4\ +K3MnO4\ +3MnO2\ +3O2}}}.
Реагирует с солями двухвалентного марганца, например:
- 2KMnO4+3MnSO4+2H2O⟶5MnO2+K2SO4+2H2SO4{\displaystyle {\ce {2KMnO4 + 3MnSO4 + 2H2O -> 5MnO2 + K2SO4 + 2H2SO4}}}.
Эта реакция в принципе обратна дисмутации (диспропорционирование) K2MnO4{\displaystyle {\ce {K2MnO4}}} на MnO2{\displaystyle {\ce {MnO2}}} и KMnO4{\displaystyle {\ce {KMnO4}}}.
Окисляет органические вещества. В частности, разбавленные растворы перманганата калия в щелочной и нейтральной среде окисляют алкены до диолов (реакция Вагнера):
Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
При смеси с пероксидом водорода протекает следующая реакция:
- 2KMnO4+3H2O2⟶2MnO2+3O2↑+2H2O+2KOH{\displaystyle {\ce {2KMnO4 +3H2O2 -> 2MnO2 + 3O2 ^ + 2H2O + 2KOH}}}.
Перманганат калия реагирует с концентрированной соляной, бромоводородной или иодоводородной кислотой. В результате выделяются свободные галогены:
- 2KMnO4+16HCl⟶2KCl+2MnCl2+5Cl2↑+8H2O{\displaystyle {\ce {2KMnO4 + 16HCl -> 2KCl + 2MnCl2 + 5Cl2 ^ + 8H2O}}}
Во время химической реакции хлорид-анион Cl−{\displaystyle {\ce {Cl^{-}}}} окисляется до элементарного хлора, а ион Mn7+{\displaystyle {\ce {Mn^{7+}}}} в перманганат-анионе восстанавливается до катиона Mn2+{\displaystyle {\ce {Mn^{2+}}}}:
- 2Cl−⟶Cl2↑{\displaystyle {\ce {2Cl^{-}-> Cl2 ^}}}
- Mn7+⟶Mn2+{\displaystyle {\ce {Mn^{7+}-> Mn^{2+}}}}
Цена Марганцовки. Где взять Перманганат калия?
Приобрести Перманганат калия непросто. В интернете много как сообщений о том, что марганцовка запрещена и найти ее очень проблематично.
На вопрос, почему запретили продажу этого средства, некоторые фармацевты отвечают, что соответствующими приказами марганцовку приравняли к взрывчатым веществам, и продавать ее без лицензии нельзя.
Другие же говорят, что марганцовокислый калий отнесен к наркотическим веществам и, опять-таки, его продажа без соответствующей лицензии невозможна.
В советах относительно того, где купить марганцовку в аптеке Москвы, обычно указывают специализированные аптеки при родильных отделениях и детских поликлиниках, а также ветеринарные аптеки.
Перманганат калия купить в Москве можно также в хозяйственных магазинах и магазинах, которые реализуют товары для садоводства.
Аналогичные рекомендации дают в ответ на вопрос, где можно купить марганцовокислый калий в СПб или Киеве.
Сколько стоит в аптеке Марганцовка? Цена средства варьируется в пределах от 11 до 165 руб. (в зависимости от объема упаковки и формы выпуска).
Образование: Окончила Ровенский государственный базовый медицинский колледж по специальности «Фармация». Окончила Винницкий государственный медицинский университет им. М.И.Пирогова и интернатуру на его базе.
Опыт работы: С 2003 по 2013 г. – работала на должностях провизора и заведующего аптечным киоском. Награждена грамотами и знаками отличия за многолетний и добросовестный труд. Статьи на медицинскую тематику публиковались в местных изданиях (газеты) и на различных Интернет-порталах.
Применение марганцовки при размножении растений
Цветоводы часто используют раствор марганцовки для обработки срезов корневищ, луковиц, клубнелуковиц. Процедуру можно проводить не только при делении и омоложении старых растений, но и для лечения поврежденных экземпляров. Раствор перманганата калия защищает цветы от болезней и вредителей, укрепляет иммунитет и предохраняет от потери влаги.
После омоложения бегоний, деления гладиолусов, георгинов или гиппеаструмов приготовьте насыщенный раствор перманганата калия и аккуратно смажьте все поверхности срезов куском ваты. Затем просушите влажные участки, присыпьте древесным углем и высаживайте растения в грунт.
Погружать луковицы и корневища в раствор не рекомендуется, чтобы оголенные части не получили ожог.
Химические свойства
| Окисленная форма | Восстановленная форма | Среда | E, В |
|---|---|---|---|
| MnO4− | MnO42− | OH− | +0,56 |
| MnO4− | H2MnO4 | H+ | +1,22 |
| MnO4− | MnO2 | H+ | +1,69 |
| MnO4− | MnO2 | OH− | +0,60 |
| MnO4− | Mn2+ | H+ | +1,51 |

Слева направо (водные растворы): Co(NO3)2 (красный); K2Cr2O7 (оранжевый); K2CrO4 (жёлтый); NiCl2 (бирюзовый); CuSO4 (голубой); KMnO4 (фиолетовый)
Раствор KMnO4 в воде в мерной колбе
Является сильным окислителем. В зависимости от pH раствора окисляет различные вещества, восстанавливаясь до соединений марганца разной степени окисления. В кислой среде — до соединений марганца(II), в нейтральной — до соединений марганца(IV), в сильно щелочной — до соединений марганца(VI). Примеры реакций приведены ниже (на примере взаимодействия с сульфитом калия):
в кислой среде:
- 2KMnO4+5K2SO3+3H2SO4⟶6K2SO4+2MnSO4+3H2O{\displaystyle {\ce {2KMnO4 + 5K2SO3 + 3H2SO4 -> 6K2SO4 + 2MnSO4 + 3H2O}}};
в нейтральной среде:
- 2KMnO4+3K2SO3+H2O⟶3K2SO4+2MnO2+2KOH{\displaystyle {\ce {2KMnO4 + 3K2SO3 + H2O -> 3K2SO4 + 2MnO2 + 2KOH}}};
в щелочной среде:
- 2KMnO4+K2SO3+2KOH⟶K2SO4+2K2MnO4+H2O{\displaystyle {\ce {2KMnO4 + K2SO3 + 2KOH -> K2SO4 + 2K2MnO4 + H2O}}}.
Однако последняя реакция (в щелочной среде) идёт по указанной схеме только при недостатке восстановителя и высокой концентрации щёлочи, которая обеспечивает замедление гидролиза манганата калия.
При соприкосновении с концентрированной серной кислотой перманганат калия взрывается, однако при аккуратном соединении с холодной кислотой реагирует с образованием неустойчивого оксида марганца(VII):
- 2KMnO4+H2SO4⟶K2SO4+Mn2O7+H2O{\displaystyle {\ce {2KMnO4 + H2SO4 -> K2SO4 + Mn2O7 + H2O}}}.
При этом в качестве промежуточного продукта может образовываться интересное соединение — оксосульфат марганца MnO3HSO4{\displaystyle {\ce {MnO3HSO4}}}. По реакции с фторидом иода(V) можно получить аналогичный оксофторид:
- KMnO4+IF5⟶KF+IOF3+MnO3F{\displaystyle {\ce {KMnO4 + IF5 -> KF + IOF3 + MnO3F}}}.
При нагревании разлагается с выделением кислорода (этим способом пользуются в лаборатории для получения чистого кислорода). Схему реакции упрощённо можно представить уравнением:
- 2KMnO4→∘tK2MnO4 +MnO2 +O2{\displaystyle {\ce {2KMnO4->K2MnO4\ +MnO2\ +O2}}}.
На самом деле реакция идёт намного сложнее, например, при не очень сильном нагревании её можно примерно описать уравнением:
- 5KMnO4→∘tK2MnO4 +K3MnO4 +3MnO2 +3O2{\displaystyle {\ce {5KMnO4->K2MnO4\ +K3MnO4\ +3MnO2\ +3O2}}}.
Реагирует с солями двухвалентного марганца, например:
- 2KMnO4+3MnSO4+2H2O⟶5MnO2+K2SO4+2H2SO4{\displaystyle {\ce {2KMnO4 + 3MnSO4 + 2H2O -> 5MnO2 + K2SO4 + 2H2SO4}}}.
Эта реакция в принципе обратна дисмутации (диспропорционирование) K2MnO4{\displaystyle {\ce {K2MnO4}}} на MnO2{\displaystyle {\ce {MnO2}}} и KMnO4{\displaystyle {\ce {KMnO4}}}.
Окисляет органические вещества. В частности, разбавленные растворы перманганата калия в щелочной и нейтральной среде окисляют алкены до диолов (реакция Вагнера):

Водные растворы перманганата калия термодинамически нестабильны, но кинетически довольно устойчивы. Их сохранность резко повышается при хранении в темноте.
При смеси с пероксидом водорода протекает следующая реакция:
- 2KMnO4+3H2O2⟶2MnO2+3O2↑+2H2O+2KOH{\displaystyle {\ce {2KMnO4 +3H2O2 -> 2MnO2 + 3O2 ^ + 2H2O + 2KOH}}}.
Перманганат калия реагирует с концентрированной соляной, бромоводородной или иодоводородной кислотой. В результате выделяются свободные галогены:
- 2KMnO4+16HCl⟶2KCl+2MnCl2+5Cl2↑+8H2O{\displaystyle {\ce {2KMnO4 + 16HCl -> 2KCl + 2MnCl2 + 5Cl2 ^ + 8H2O}}}
Во время химической реакции хлорид-анион Cl−{\displaystyle {\ce {Cl^{-}}}} окисляется до элементарного хлора, а ион Mn7+{\displaystyle {\ce {Mn^{7+}}}} в перманганат-анионе восстанавливается до катиона Mn2+{\displaystyle {\ce {Mn^{2+}}}}:
- 2Cl−⟶Cl2↑{\displaystyle {\ce {2Cl^{-}-> Cl2 ^}}}
- Mn7+⟶Mn2+{\displaystyle {\ce {Mn^{7+}-> Mn^{2+}}}}
Взаимодействие
Марганцовокислый калий химически несовместим с рядом органических веществ (включая танин, сахар, уголь).
Взрывается при обработке концентрированной H2SО4 (серной кислотой).
Даже при незначительном (до комнатной температуры) нагреве активно взаимодействует с большинством восстановителей (например, с глицерином) и легкоокисляющимися веществами. Реакция сопровождается саморазогреванием, что в ряде случаев вызывает самовоспламеняющиеся смеси и может привести к взрыву.
Очень опасно растирать кристаллы марганцовокислого калия с порошками активных металлов и неметаллов (алюминием, серой, кальцием, фосфором, магнием и др.), поскольку подобные действия нередко сопровождаются взрывом.
Как развести марганцовку для обработки в медицинских целях
Главное правило – соблюдать четкие пропорции во время приготовления раствора, иначе марганцовка станет опасным раздражителем для кожи и слизистых. Для обработки чаще всего применяют 0,1-0,5%-ный раствор. Самый слабый раствор марганцовки используют для полосканий рта и горла. Наружные гнойные раны, ожоги допустимо смазывать 2%-ным составом.
Для приготовления слабого раствора на 1 л воды добавьте 2-3, более крепкого – 3-4 крупинки вещества. Чтобы они быстрее растворились, можно использовать теплую воду.
Раствор марганцовки для любых процедур всегда должен быть свежим
Во время приготовления раствора обязательно соблюдайте следующие правила безопасности:
- не трогайте руками крупинки марганцовки, а берите их ложкой, спичкой или зубочисткой;
- тщательно размешивайте раствор до полного растворения крупинок, чтобы не получить ожог;
- не храните готовый раствор;
- используйте индивидуальные средства защиты во время работы с препаратом.
Храните перманганат калия в недоступных для детей и животных местах. Не оставляйте вещество на солнце.









